Theo khuyến nghị của Ban cố vấn, việc chấp thuận vaccine Covid-19 của Pfizer có thể bắt đầu trong vòng vài ngày tới, tùy thuộc vào tốc độ xử lý của FDA.
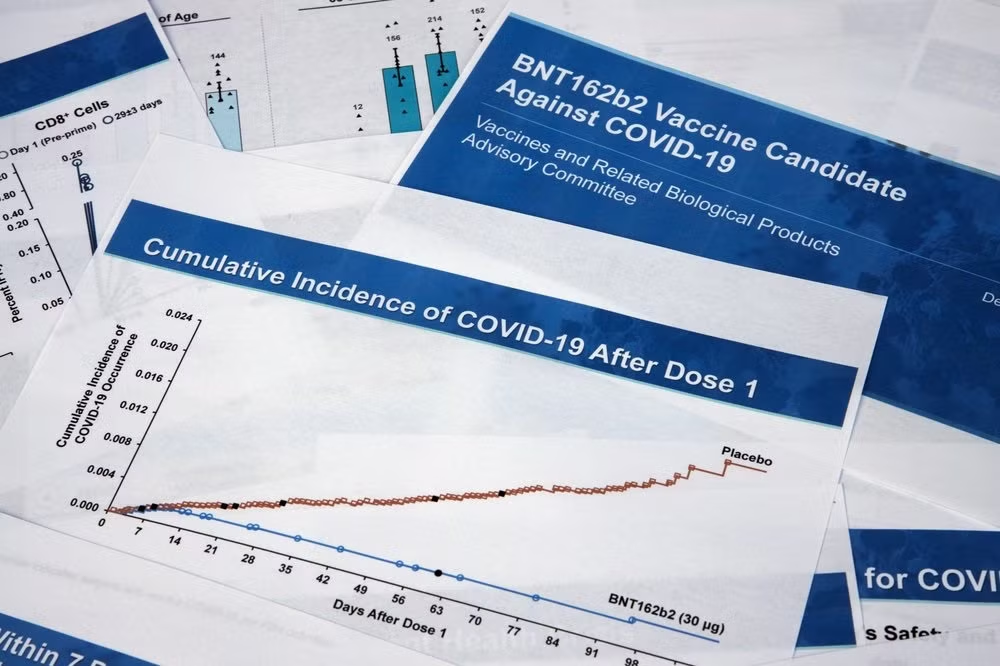
Cuộc bỏ phiếu có 17 phiếu thuận, bốn phiếu chống và một phiếu trắng. Các chuyên gia kết luận rằng vaccine từ Pfizer và đối tác BioNTech của Đức có vẻ an toàn và hiệu quả để sử dụng khẩn cấp ở người lớn và thanh thiếu niên từ 16 tuổi trở lên.
Sự chứng thực đó được đưa ra bất chấp những băn khoăn về phản ứng dị ứng ở hai người được tiêm vaccine vào đầu tuần này ở Anh.
Tiến sĩ Paul Offit, Bệnh viện Nhi Philadelphia, thành viên hội đồng cố vấn cho rằng, vẫn còn một số điều chưa biết về vaccine để sử dụng trong trường hợp khẩn cấp. Nhưng ông kết luận, lợi ích tiềm năng lớn hơn rủi ro.
Quyết định này được đưa ra khi các trường hợp mắc Covid-19 tăng lên ngày càng cao trên khắp nước Mỹ. Ngày 9-12, số ca tử vong ở Mỹ lập kỷ lục mọi thời đại, với hơn 3.100 ca.
Pfizer cho biết sẽ có khoảng 25 triệu liều vaccine hai mũi cung cấp cho Mỹ vào cuối tháng 12. Nhưng nguồn cung cấp ban đầu sẽ chủ yếu dành cho nhân viên chăm sóc sức khỏe và người già ở viện dưỡng lão, các nhóm dễ bị tổn thương khác sẽ được lần lượt tiêm tiếp theo cho đến khi việc sản xuất vaccine đáp ứng nhu cầu tiêm chủng rộng rãi, nhưng điều có thể sẽ không xảy ra trước mùa xuân.
Tuần tới, FDA sẽ xem xét loại vaccine thứ hai của Moderna có hiệu quả phòng ngừa như vaccine của Pfizer-BioNTech. Ứng cử viên thứ ba là của Johnson & Johnson chỉ cần một liều tiêm, đang hoạt động theo cách của mình. Xếp sau là ứng viên đến từ AstraZeneca và Đại học Oxford.
Các chuyên gia y tế Mỹ đang hy vọng sự kết hợp của các loại vaccine cuối cùng sẽ giúp nước này có thể chiến thắng dịch bệnh bùng phát.
Tuy nhiên, các chuyên gia ước tính ít nhất 70% dân số Mỹ sẽ phải tiêm phòng để đạt được khả năng miễn dịch bầy đàn, thời điểm mà virus có thể được kiểm soát.
Mọi con mắt đang đổ dồn về các nhà khoa học của FDA, những người sẽ đưa ra quyết định cuối cùng về việc có nên tiến hành chủng ngừa quy mô lớn với vaccine của Pfizer-BioNTech hay không. Giám đốc vaccine của FDA, Tiến sĩ Peter Marks cho biết sẽ có quyết định trong vòng “vài ngày đến một tuần”.
Tiến sĩ Patrick Moore, Đại học Pittsburgh cho biết: “Mặc dù hiệu quả riêng lẻ của loại vaccine này là rất, rất rất cao, nhưng hiện tại vẫn chưa có bất kỳ bằng chứng nào cho thấy nó sẽ làm giảm khả năng lây lan”. Ông thúc giục Pfizer thực hiện các bước bổ sung để trả lời câu hỏi đó.
Một số thành viên hội đồng bất đồng chính kiến đã phản đối việc cấp phép tiêm cho thanh niên 16 và 17 tuổi, do trong nghiên cứu, đối tượng này mới chiếm số lượng nhỏ và họ có nguy cơ thấp với Covid-19.