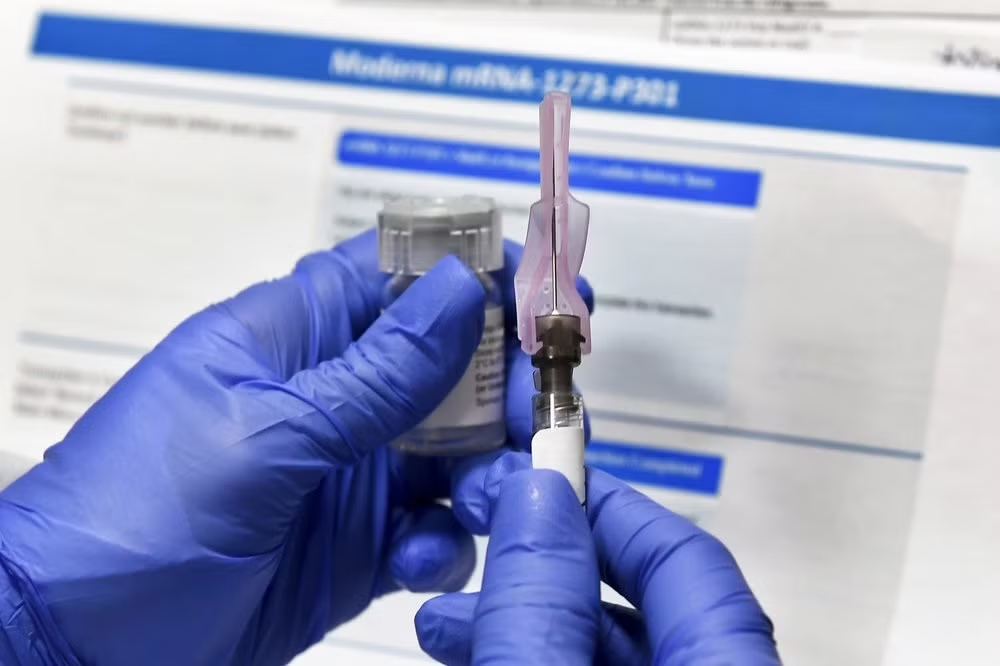
Sau khi các chuyên gia tán thành, Cục Quản lý thực phẩm và dược phẩm Mỹ (FDA) dự kiến sẽ cấp phép sử dụng khẩn cấp (EUA) cho loại vaccine của Moderna và Viện Y tế Quốc gia Mỹ phát triển, và nó sẽ trở thành vaccine thứ hai được sử dụng tại Mỹ.
Khi được cấp phép sử dụng khẩn cấp, Moderna sẽ bắt đầu vận chuyển hàng triệu liều, dành riêng cho nhân viên y tế và cư dân viện dưỡng lão, để thúc đẩy nỗ lực tiêm chủng lớn nhất trong lịch sử nước Mỹ.
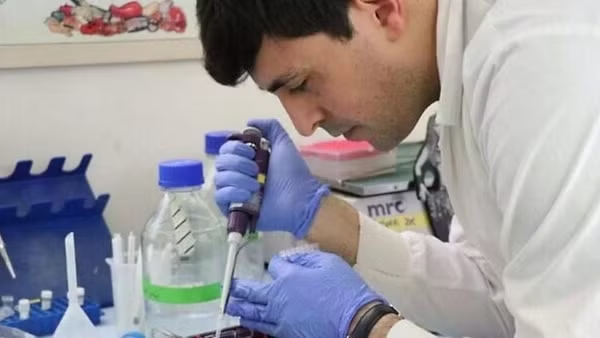
Chiến dịch tiêm chủng bắt đầu vào đầu tuần này với vaccine đầu tiên được phê duyệt ở Mỹ, do Pfizer và BioNTech phát triển. Vaccine của Moderna cho thấy có hiệu quả mạnh tương tự, cung cấp 94% khả năng chống lại Covid-19 trong thử nghiệm liên tục của công ty với 30.000 người.
Sau tám giờ thảo luận, hầu hết các thành viên tham gia hội thảo đều ủng hộ việc sử dụng vaccine của Moderna để chống lại đại dịch. Một thành viên ban hội thẩm đã bỏ phiếu trắng.
Tiến sĩ Hayley Gans của Trung tâm Y tế Đại học Stanford cho biết: “Bằng chứng đã được nghiên cứu rất chi tiết về loại vaccine này vượt trội hơn bất kỳ vấn đề nào mà chúng tôi đã thấy”.
Việc phê duyệt khẩn cấp loại vaccine thứ hai tại Mỹ là cần thiết vì các ca mắc Covid-19, nhập viện và tử vong tăng lên mức cao mới trước kỳ nghỉ lễ. Mỹ dẫn đầu thế giới về tổng số người mắc Covid-19, với hơn 1,6 triệu trường hợp được xác nhận và hơn 310.000 trường hợp tử vong được báo cáo.

Vaccine Covid-19 của Moderna sử dụng công nghệ đột phá tương tự như vaccine của Pfizer-BioNTech. Hầu hết các loại vaccine truyền thống đều sử dụng virus đã chết hoặc làm yếu đi, nhưng cả hai loại vaccine mới đều sử dụng các đoạn mã di truyền của Covid-19 để huấn luyện hệ thống miễn dịch phát hiện và chống lại virus. Cả hai loại vaccine đều cần tiêm hai liều, trong khi vaccine của Pfizer hai liều cách nhau hai tuần thì vaccine của Moderna cách nhau bốn tuần.
Cuộc bỏ phiếu tán thành vaccine của Moderna diễn ra vài ngày sau khi có báo cáo về phản ứng dị ứng rõ ràng với vaccine Pfizer-BioNTech ở hai nhân viên y tế Alaska, Mỹ. Một người bị phản ứng nghiêm trọng với triệu chứng khó thở, người còn lại có các phản ứng phụ ít nghiêm trọng hơn với biểu hiện choáng váng.
Tiến sĩ Tal Zaks, Giám đốc y tế của Moderna cho rằng, mặc dù hai loại vaccine sử dụng cùng một công nghệ nhưng chúng không giống nhau. Đặc biệt, một số chất được sử dụng để phủ hai loại vaccine là khác nhau.
“Theo tôi, không nhất thiết phải cho rằng mọi phản ứng sẽ giống nhau”, ông nói.
FDA không tìm thấy phản ứng dị ứng nghiêm trọng trong dữ liệu của Moderna nhưng có dấu hiệu của các tác dụng phụ ít nghiêm trọng hơn như phát ban, nổi mề đay, ngứa ở những người tham gia tiêm vaccine, so với những người được tiêm giả dược.
Trong số những người tiêm thử nghiệm vaccine của Moderna cũng có ba trường hợp bị liệt cơ mặt tạm thời, so với chỉ một trong số những người được tiêm giả dược. Tuy nhiên, đánh giá của FDA cho biết, vai trò của vaccine Moderna trong nhóm vaccine ngừa Covid-19 là "không thể bị loại trừ."
Ông Doran Fink, quan chức FDA cho biết, nếu vaccine của Moderna được phê duyệt sử dụng khẩn cấp, cơ quan này sẽ phát hành cảnh báo bổ sung liên quan đến các phản ứng dị ứng tiềm ẩn.
Một băn khoăn nữa chưa được trả lời là liệu vaccine của Moderna có ngăn ngừa được nhiễm Covid-19 không có triệu chứng ở người hay không, nhưng Moderna đã đưa ra một dữ liệu cho rằng điều này là có thể. Những người tham gia thử nghiệm được xét nghiệm dịch mũi trước khi tiêm liều thứ hai của vaccine hoặc giả dược. Tiến sĩ Jacqueline Miller của Moderna cho biết, tại thời điểm đó, các mẫu gạc từ 14 người nhận vaccine và 38 người nhận giả dược cho thấy bằng chứng nhiễm Covid-19 không có triệu chứng.
Moderna chỉ mới bắt đầu thử nghiệm vaccine của mình ở trẻ em từ 12 đến 17 tuổi. Việc thử nghiệm ở trẻ nhỏ hơn dự kiến sẽ bắt đầu vào đầu năm tới.
Sau khi FDA phê duyệt vaccine thứ hai, Mỹ có kế hoạch chuyển lô hàng ban đầu gồm gần 6 triệu liều vaccine của Moderna. Vaccine này cần bảo quản ở nhiệt độ tủ đông thông thường, chứ không cần nhiệt độ cực lạnh như mũi tiêm của Pfizer-BioNTech.
Với việc bổ sung vaccine Moderna, các quan chức chính phủ dự đoán, 20 triệu người Mỹ sẽ có thể tiêm mũi đầu tiên vào cuối tháng 12 và 30 triệu người nữa được tiêm vào tháng 1-2021.






















![[Infographic] Kết quả công tác tiếp nhận đơn và bảo hộ chỉ dẫn địa lý giai đoạn 2021-2025](https://cdn.nhandan.vn/images/d1cf90f5c1991127e08583db2f458887e115c8f07c5898c5027d2f112d5c985bec09598c537ebba8d4fab4fd468cf41d/gcn-1.png.avif)

