Trong đó, các đơn vị báo cáo về khả năng cung ứng test xét nghiệm SARS-CoV-2 (tên, chủng loại test xét nghiệm; hãng, nước sản xuất/cung ứng; thông tin về lưu hành sản phẩm; thông số kỹ thuật của sản phẩm; khả năng cung ứng theo tháng; giá bán theo đơn vị đóng gói nhỏ nhất (đồng); các thông tin khác liên quan).
Đồng thời, báo cáo về các khó khăn, vướng mắc trong quá trình thực hiện sản xuất/nhập khẩu test xét nghiệm SARS-CoV-2 (nếu có).
Bộ Y tế đề nghị các cơ sở ký, tên đóng dấu các văn bản, tài liệu gửi về Bộ Y tế trước 16 giờ ngày 17/10/2021 và các cơ sở chịu trách nhiệm trước pháp luật về tính chính xác, hợp pháp của toàn bộ thông tin công bố với Bộ Y tế.
Bộ Y tế sẽ tổng hợp và báo cáo Chính phủ đồng thời thông báo cho các đơn vị, địa phương thông tin test xét nghiệm SARS-CoV-2 (đã được cấp phép) để tham khảo trong quá trình quyết định mua test xét nghiệm SARS-CoV-2.
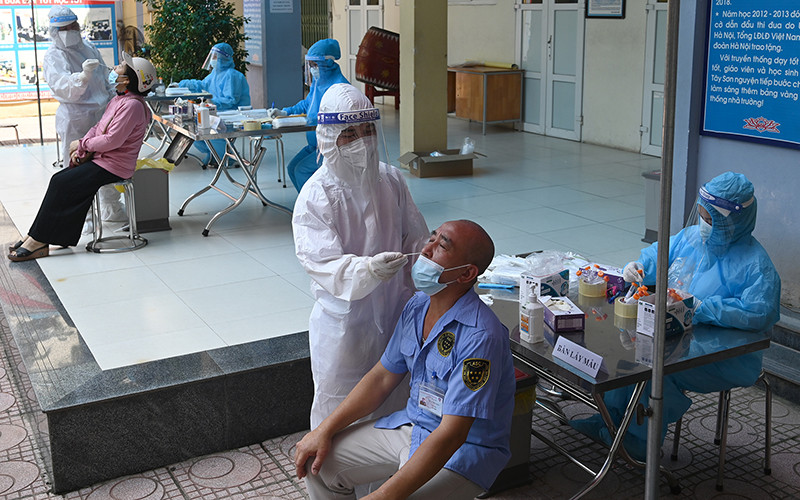
Trước tình hình diễn biến phức tạp của dịch bệnh viêm đường hô hấp cấp do chủng mới của virus corona (SARS-CoV-2) gây ra (dịch Covid-19) và yêu cầu xét nghiệm SARS-CoV-2 phục vụ phòng, chống dịch Covid-19 hiện nay, Bộ Y tế khuyến khích và ủng hộ các cơ sở sản xuất và kinh doanh tìm kiếm nguồn hàng trang thiết bị y tế/sinh phẩm chẩn đoán in vitro chẩn đoán xét nghiệm SARS-CoV-2 (test xét nghiệm SARS-CoV-2) chất lượng, tin cậy, giá thành hợp lý, bảo đảm cung ứng đủ cho nhu cầu xét nghiệm phục vụ phòng, chống dịch Covid-19.














![[Video] Bộ Y tế tiếp tục rà soát, mở rộng danh mục thuốc bảo hiểm y tế](https://cdn.nhandan.vn/images/aefb60fa2e0040d9e6860d421bf1805038abc5dc41fcafa38f0ad810d3d060608785607d4acd935919ec4d7bbdab70887ae152c91a8510b1275a06b509524cf960a83bd4d8652413b4c07144236690ad187cfe43b7b2feb88ca5588a6d87599d29adcb54e1a58315ae5146673abc75d7/720.jpg.webp)