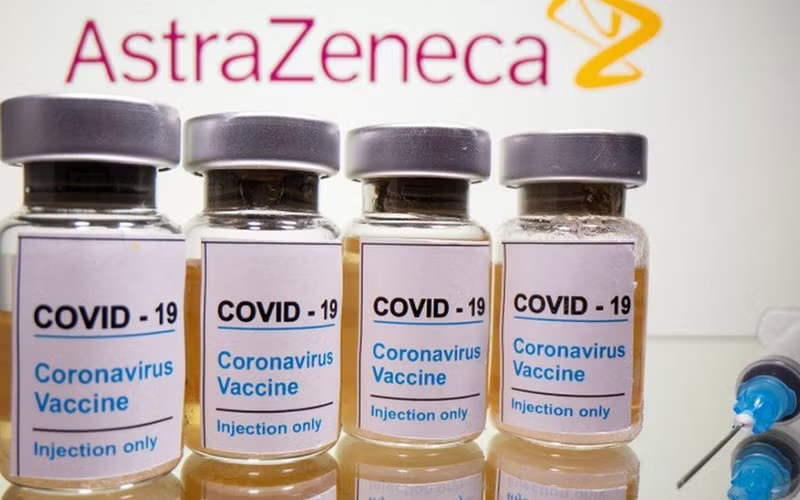
Bộ Y tế đã ban hành Quyết định số 983/QĐ-BYT phê duyệt có điều kiện vaccine cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 theo quy định tại Điều 67, Nghị định số 54/2017/NĐ-CP ngày 8-5-2017 của Chính phủ quy định chi tiết một số điều kiện và biện pháp thi hành Luật Dược.
Vaccine AstraZeneca có hoạt chất, nồng độ/hàm lượng mỗi liều (0,5ml) chứa vaccine Covid-19 (ChAdOxl-S tái tổ hợp) 5 x 10" hạt virus (vp).
Vaccine do Catalent Anagni S.R.L-Y; CP Pharmaceuticals Limited - Anh.l; IDT Biologika GmbH - Đức sản xuất. Cơ sở sản xuất có thể được thay đổi căn cứ vào khả năng cung cấp vaccine tại thời điểm cơ sở nhập khẩu nộp hồ sơ đề nghị cấp phép nhập khẩu vaccine theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP. Cơ sở đề nghị phê duyệt vaccine là Công ty TNHH AstraZeneca Việt Nam.
Theo quyết định này, Cục Quản lý Dược có trách nhiệm cấp phép nhập khẩu vaccine Covid-19 vaccine AstraZeneca theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP khi nhận được hồ sơ của cơ sở nhập khẩu. Thực hiện đúng quy định của pháp luật về quản lý nhập khẩu, quản lý chất lượng vaccine nhập khẩu.
Cục Khoa học Công nghệ và Đào tạo có trách nhiệm làm đầu mối triển khai đánh giá lâm sàng tại Việt Nam về tính an toàn và tính sinh miễn dịch của vaccine Covid-19 AstraZeneca.
Cục Y tế Dự phòng có trách nhiệm xây dựng kế hoạch tiêm chủng và tổ chức triển khai, hướng dẫn tiêm chủng, giám sát trong quá trình tiêm chủng, theo dõi phản ứng sau tiêm chủng và tổ chức việc báo cáo, tổng hợp thông tin, dữ liệu tiêm chủng vaccine phòng Covid-19 AstraZeneca.
Viện Kiểm định quốc gia vaccine và sinh phẩm y tế có trách nhiệm tiến hành kiểm định vaccine Covid-19 AstraZeneca trước khi đưa ra sử dụng.
![[Video] Bức xạ tia X ảnh hưởng cơ thể người thế nào - Phần 1](https://cdn.nhandan.vn/images/aefb60fa2e0040d9e6860d421bf1805017dfc746e5d5ac832f13d36cc1171a4ea5d9a5fc89a5388679b1bdf0ca7ac94752623ff52aeffd6a264ec6cf75e3718fb04ba1fb63f932a4702d70e1ae25e2dc/avatar-of-video-1160961-2810.png.avif)










![[Video] Ca ngộ độc thực phẩm cả nước tăng vọt](https://cdn.nhandan.vn/images/fe9e98de2d487cb794d38ce785269d0f263b27e1212cd33212a714767e25aff11071a675080f79e5915cb1538491a10be667d376bf869970b83bd2a9ea12e0ea/ngo-doc.jpg.avif)