Các thuốc phát minh chỉ chiếm khoảng 3%
Theo Bộ Y tế, Việt Nam đã có 230 nhà máy đạt tiêu chuẩn GMP-WHO, trong đó có gần 20 nhà máy đạt GMP-EU. Tổ chức Y tế thế giới (WHO) phân loại công nghiệp dược nước ta thuộc nhóm mức độ 3, sản xuất được bản sao của biệt dược (thuốc generic) và tự chủ một phần thuốc chữa bệnh. Năm 2023-2024, quy mô thị trường dược phẩm đạt 6,5 - 7 tỷ USD, trong đó nhập khẩu 3,5 tỷ USD. Xuất khẩu dược còn khiêm tốn, mới đạt hơn 200 triệu USD; nguyên liệu hóa dược phải nhập khẩu khoảng 90%.
Nguyên nhân chủ yếu là quy mô của cơ sở sản xuất dược phẩm trong nước hiện nay phần lớn là doanh nghiệp vừa và nhỏ, chưa chú trọng đầu tư nghiên cứu sản xuất, chuyển giao các thuốc nói trên do cần nguồn lực lớn về tài chính, thời gian, nhân lực chất lượng cao. Việc đầu tư cho nghiên cứu phát triển cũng còn rất khiêm tốn, chủ yếu là các dạng thuốc thông thường; chưa chú trọng nghiên cứu, sản xuất thuốc dạng bào chế hiện đại, tối ưu hóa công thức và quy trình sản xuất.
Cục trưởng Quản lý Dược Vũ Tuấn Cường nhận định, trước đây chúng ta khuyến khích sản xuất thuốc generic, bảo đảm thuốc thiết yếu, do đó, doanh nghiệp chưa chú trọng nghiên cứu sản xuất thuốc công nghệ cao, thuốc mới, thuốc chuyên khoa đặc trị, thuốc phát minh. Do vậy, cần xây dựng cơ chế, chính sách khuyến khích đủ mạnh để thu hút doanh nghiệp, nhà đầu tư nhằm thúc đẩy hoạt động đầu tư nghiên cứu, phát triển công nghệ mới sản xuất các thuốc thuộc diện cần ưu tiên phát triển theo đề xuất tại dự thảo sửa đổi Luật Dược.
 |
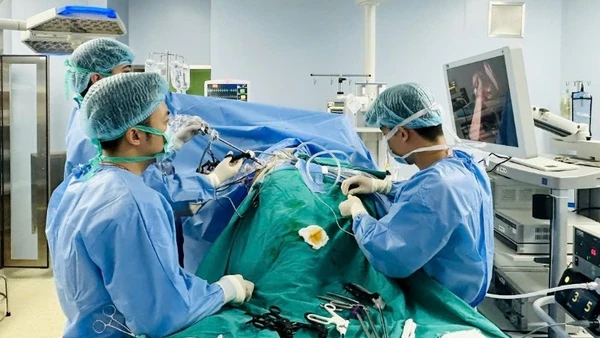
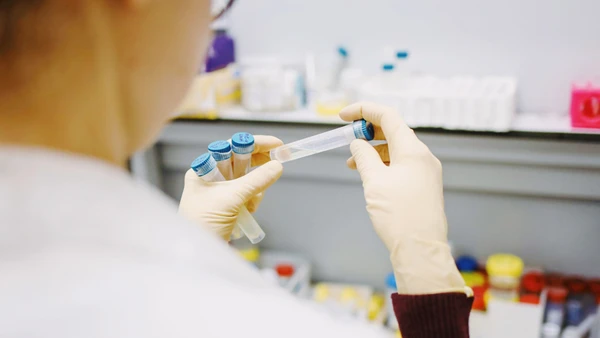
| Các hãng dược trong nước ngày càng kiện toàn khâu sản xuất để cạnh tranh trực tiếp với dược phẩm nhập ngoại. Ảnh: Imexpharm |
Cải thiện thủ tục pháp lý nhằm thúc đẩy sản xuất
Theo Cục Quản lý Dược, dự thảo Luật Dược sửa đổi đã đề xuất các quy định theo hướng khuyến khích sản xuất thuốc phát minh, thuốc có dạng bào chế công nghệ cao, thay vì sản xuất thuốc generic như trong thời gian qua. Đây được kỳ vọng tạo bước bứt phá cho công nghiệp dược trong nước.
Cụ thể, tại dự thảo sửa đổi bổ sung Luật Dược, Bộ Y tế đã đề xuất sửa đổi, bổ sung khoản 3 điều 7 của Luật Dược, với nhiều ưu đãi đặc biệt về đầu tư; chính sách thuế, vay vốn, ưu đãi; hỗ trợ về thủ tục hành chính liên quan đến đầu tư, cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc; các chính sách hỗ trợ đầu tư khác theo quy định của pháp luật đối với các hoạt động đầu tư sản xuất nguyên liệu làm thuốc, sản xuất thuốc mới, thuốc biệt dược gốc, thuốc ứng dụng công nghệ cao trong sản xuất, thuốc chuyên khoa đặc trị được chuyển giao công nghệ sản xuất tại Việt Nam...; ưu đãi nghiên cứu khoa học về công nghệ bào chế, công nghệ sinh học để sản xuất các loại thuốc mới...
Theo các chuyên gia, quy định ưu đãi toàn diện được thể hiện tại dự thảo Luật Dược sửa đổi là nền tảng quan trọng giúp thúc đẩy các doanh nghiệp đầu tư mạnh mẽ vào lĩnh vực dược phẩm, nhất là đối với các loại thuốc có giá trị cao và công nghệ phức tạp. Tuy nhiên, điều quan trọng hơn là sau khi ban hành, các chính sách này phải thật sự đi vào cuộc sống.
Ông Trịnh Lương Ngọc, luật sư thành viên của Công ty Luật VILAF cho biết, trong quá trình tư vấn pháp lý cho các doanh nghiệp, khó khăn phổ biến mà các doanh nghiệp gặp phải là do quy định pháp luật chưa đồng bộ và thủ tục hành chính phức tạp.
Ông Ngọc khuyến nghị, Bộ Y tế cần cải cách ngay thủ tục hành chính để thúc đẩy quá trình đổi mới, sáng tạo hay chuyển giao công nghệ được thực hiện kịp thời hơn, hỗ trợ cho chính các doanh nghiệp nhận chuyển giao trong nước và doanh nghiệp nước ngoài. Cụ thể, triển khai nhanh các bước đơn giản hóa thủ tục đăng ký và gia hạn giấy đăng ký lưu hành thuốc để doanh nghiệp có thể nhanh chóng đăng ký và đưa sản phẩm ra thị trường, thúc đẩy cạnh tranh và giúp người dân tiếp cận thuốc sớm hơn. Đặc biệt, cần rút ngắn thời gian cấp phép và triển khai các dự án đầu tư có quy mô lớn.
Trên thực tế, việc triển khai các dự án có quy mô lớn thường kéo dài nhiều năm, từ giai đoạn lập báo cáo tiền khả thi (pre-FS), cấp phép đầu tư, giải tỏa và giao đất, đến xây dựng và đưa vào hoạt động. Quá trình kéo dài và chậm trễ này khiến các tập đoàn lớn trên thế giới phải cân nhắc kỹ lưỡng trước khi quyết định đầu tư các dự án lớn tại Việt Nam.
Các chuyên gia nhấn mạnh, để ngành dược Việt Nam phát triển, có ba yếu tố quan trọng cần tập trung: Thứ nhất, tạo ra một môi trường thuận lợi hơn với hoạt động đầu tư thông qua các chính sách rõ ràng, bền vững để tạo động lực cho các doanh nghiệp ưu tiên đưa các liệu pháp tiên tiến đến Việt Nam sớm hơn cũng như sẵn sàng đầu tư dài hạn. Thứ hai, đưa ra các chính sách ưu đãi ưu tiên lĩnh vực đổi mới, phát minh, khuyến khích đầu tư vào các giai đoạn sớm của quy trình nghiên cứu, phát triển sản phẩm như nghiên cứu lâm sàng và nâng cao năng lực sản xuất. Thứ ba, cần có một quy trình thực hiện chiến lược quốc gia phát triển ngành dược hiệu quả.
Thuốc phát minh là sản phẩm thuốc có chứa dược chất mới do các nhà nghiên cứu hoặc các nhà sản xuất sáng chế ra. Hãng dược đứng tên bằng phát minh được phép sản xuất độc quyền sản phẩm trong một thời gian nhất định (thường từ 10 đến 20 năm kể từ ngày dược chất được tìm thấy).