Cục An toàn thực phẩm (Bộ Y tế) vừa ban hành các quyết định thu hồi hiệu lực Giấy tiếp nhận bản đăng ký công bố sản phẩm đối với hàng loạt thực phẩm chức năng của 4 công ty
Theo đó, 4 công ty bị thu hồi hiệu lực Giấy tiếp nhận đăng ký sản phẩm của một số thực phẩm bảo vệ sức khỏe gồm: Công ty Cổ phần Dược phẩm Nano Pharma, Công ty Cổ phần Kingphar Việt Nam, Công ty TNHH Thương mại & Dược phẩm Nguyễn Minh, Công ty TNHH Sản xuất & Thương mại Vinh Thịnh Vượng.
Cụ thể, tại Quyết định số 1450/QĐ-ATTP, Cục An toàn thực phẩm quyết định thu hồi hiệu lực Giấy tiếp nhận đăng ký bản công bố sản phẩm đối với sản phẩm thực phẩm bảo vệ sức khỏe Kingphar Super Kid, số Giấy tiếp nhận đăng ký bản công bố sản phẩm 13714/2019/ĐKSP cấp ngày 24/12/2019 .
Sản phẩm do Công ty TNHH Sản xuất & Thương mại Vinh Thịnh Vượng, địa chỉ: thôn Bình Phú, xã Yên Phú, huyện Yên Mỹ, tỉnh Hưng Yên công bố.
Tại Quyết định số 313/QĐ-ATTP ngày 2/7/2025, Cục An toàn thực phẩm quyết định thu hồi hiệu lực Giấy tiếp nhận đăng ký bản công bố sản phẩm đối với sản phẩm thực phẩm bảo vệ sức khỏe Enterovina số Giấy tiếp nhận đăng ký bản công bố sản phẩm 5803/2019/ĐKSP cấp ngày 23/5/2019.
Sản phẩm này do Công ty TNHH Thương mại & Dược phẩm Nguyễn Minh, địa chỉ: số nhà 45 ngõ 79, tổ 28, phường Quan Hoa, quận Cầu Giấy, thành phố Hà Nội công bố.
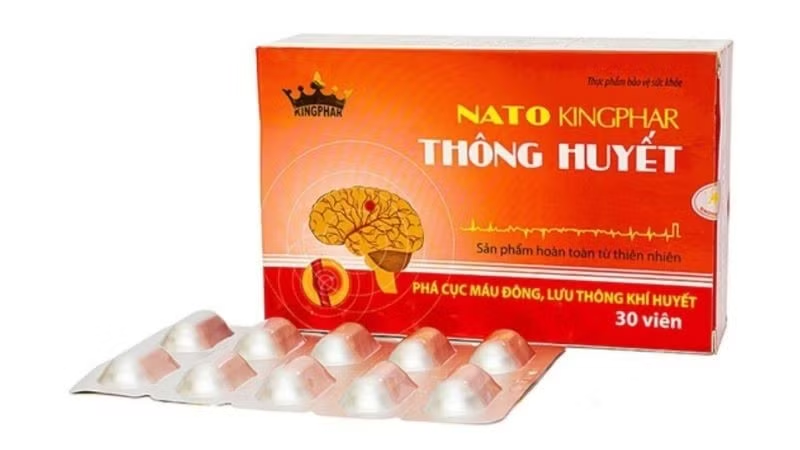
Tại Quyết định số 314/QĐ-ATTP ngày 2/7/2025, Cục An toàn thực phẩm quyết định thu hồi hiệu lực Giấy tiếp nhận đăng ký bản công bố sản phẩm đối với 4 sản phẩm thực phẩm bảo vệ sức khỏe do Công ty Cổ phần Kingphar Việt Nam, địa chỉ: thôn Bình Phú, xã Yên Phú, huyện Yên Mỹ, tỉnh Hưng Yên công bố.
Các sản phẩm này bao gồm: Nato Thông huyết-Kingphar; Menmoren ginkgo Plus; Ống uống Men tiêu hóa và Omega 3-6-9 Plus Q10 Kingphar.
Tại Quyết định số 315/QĐ-ATTP ngày 2/7/2025, Cục An toàn thực phẩm quyết định thu hồi hiệu lực Giấy tiếp nhận đăng ký bản công bố sản phẩm đối với 2 sản phẩm thực phẩm bảo vệ sức khỏe do Công ty Cổ phần Dược phẩm Nano Pharma, có địa chỉ tại số 9 Nguyễn Xiển, phường Thanh Xuân Trung, quận Thanh Xuân, thành phố Hà Nội công bố.
2 sản phẩm này gồm Nano IQ Mama Care (viên uống cho mẹ bầu) và Nano IQ Aquamin F (sản phẩm bổ sung calci và vitamin).
Theo Cục An toàn thực phẩm, các quyết định trên được đưa ra căn cứ vào văn bản của các công ty về việc xin rút hồ sơ liên quan đến tới các sản phẩm trên.





![[Video] Đề xuất mỗi trạm y tế cấp xã có 15 người, tăng theo dân số](https://cdn.nhandan.vn/images/3883af5deaaac3167e637b7d16f14779e6f22e8c2ba788d9e5c46e8ab4a4a4e223270eb5a6dce6a851c7910f41ba1498/y-te.jpg.avif)








![[Video] Phát hiện sớm bệnh nguy hiểm bằng chẩn đoán hình ảnh - Phần 2](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f52083899909c81ccf4c3aa38d2cb1b0b3410dc7892cff55400431bcae069a4acbd41a6c5eb84419e601652c0845f30bf7a25dd0d78c5f9ac818fb5639b9ba0160960f78/avatar-of-video-1169947-766.png.avif)
![[Video] Phát hiện sớm bệnh nguy hiểm bằng chẩn đoán hình ảnh - Phần 1](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f52083899909c81ccf4c3aa38d2cb1b0b3410dc7892cff55400431bcae069a4acbd41a6ca372a3fad8c671cbbad9f775e32128e484e4521323f1eae7f68017a36356e093/avatar-of-video-1169944-1261.png.avif)
![[Video] Quy trình tầm soát mạch máu não hiệu quả, tiết kiệm](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f52083899909c81ccf4c3aa38d2cb1b0b3410dc7892cff55400431bcae069a4acbd41a6cd4ae1f40403cb9b071e5d3c6a86c4ec0b592a06e22cbc4ee404dbd54b5065230/avatar-of-video-1169940-674.png.avif)
![[Video] Mẹ bầu có được chụp chiếu khi mang thai?](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f52083899909c81ccf4c3aa38d2cb1b0b3410dc7892cff55400431bcae069a4acbd41a6cbbd1eaab74b7545946a747dc37eddefbaddaa7052c7f7b2a46c9a3a2951e64af/avatar-of-video-1169949-1805.png.avif)