Cục Quản lý Dược (Bộ Y tế) vừa có công văn khẩn gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương; các bệnh viện, viện có giường bệnh trực thuộc Bộ; Viện Vệ sinh dịch tễ Trung ương; Viện Pasteur TP Hồ Chí Minh; Viện Pasteur Nha Trang; Viện Vệ sinh dịch tễ Tây Nguyên.
Công văn nêu rõ, gần đây trên các phương tiện thông tin đại chúng có đưa tin về vụ bê bối vaccine gây chấn động Trung Quốc. Theo đó, Công ty sản xuất vaccine Changsheng Biotechnology, có trụ sở tại thành phố Trường Xuân, tỉnh Cát Lâm, Trung Quốc bị phát hiện vi phạm các tiêu chuẩn trong sản xuất vaccine phòng bệnh dại ở người và đã bị cơ quan quản lý dược phẩm Trung Quốc thu hồi giấy phép sản xuất vaccine phòng dại, tiến hành điều tra hình sự.
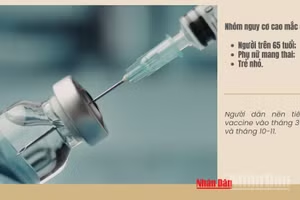
Do đó, Cục Quản lý Dược cho biết, hiện nay chỉ có một loại vaccine phòng bệnh dại sản xuất tại Trung Quốc được cấp số đăng ký và lưu hành tại Việt Nam là vaccine Speeda (số đăng ký QPVX-1041-17) do Công ty Liaon1ng cheng da biotechnology Co.,Ltd, Trung Quốc sản xuất. Vaccine này vẫn đang tiếp tục được sản xuất và cung ứng ra thị trường các nước trong đó có Việt Nam, do Công ty Trách nhiệm hữu hạn Dược phẩm Biển Loan đăng ký, nhập khẩu và không phải là vaccine trong vụ bê bối tại Trung Quốc mà gần đây các phương tiện thông tin đại chúng đưa tin.
Để tránh gây hoang mang dư luận cũng như bảo đảm công tác tiêm chủng cho nhu cầu của nhân dân, Cục Quản lý Dược yêu cầu Sở Y tế các tỉnh, thành phố trực thuộc Trung ương khẩn trương có văn bản chỉ đạo Trung tâm Kiểm soát bệnh truyền nhiễm, Trung tâm y tế dự phòng và các cơ sở tiêm chủng trên địa bàn thông báo tại các điểm tiêm chủng về việc phòng bệnh dại Speeda hiện đang lưu hành tại Việt Nam do Công ty Liaon1ng cheng da biotechnology Co.,Ltd, Trung Quốc sản xuất không phải là vaccine trong vụ bê bối tại Trung Quốc mà gần đây các phương tiện thông tin đại chúng đưa tin.
Các bệnh viện, viện có giường trực thuộc Bộ Y tế có thực hiện hoạt động tiêm vaccine phòng bệnh não mô cầu, Viện Vệ sinh dịch tễ Trung ương, Viện Pasteur TP Hồ Chí Minh, Viện Pasteur Nha Trang, Viện Vệ sinh dịch tễ Tây Nguyên cũng thông báo tại các điểm tiêm chủng về nội dung này.
“Các tỉnh, thành phố tiếp tục sử dụng vaccine Speeda nói trên để đáp ứng nhu cầu tiêm chủng của nhân dân, tránh gián đoạn tiêm chủng”, Cục Quản lý Dược yêu cầu.
* Việt Nam không lưu hành vaccine phòng dại của Công ty Changsheng Biotechnology, Trung Quốc
![[Video] Bộ Y tế yêu cầu điều tra vụ 46 người nghi ngộ độc thực phẩm tại Quảng Trị](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f5208389ab46d90823d93e7d25cbe4d7e80be5aa2662c6c7efc26fa613d671d00556dec6/ngo-doc.png.avif)






![[Video] Đề xuất mỗi trạm y tế cấp xã có 15 người, tăng theo dân số](https://cdn.nhandan.vn/images/3883af5deaaac3167e637b7d16f14779e6f22e8c2ba788d9e5c46e8ab4a4a4e223270eb5a6dce6a851c7910f41ba1498/y-te.jpg.avif)








![[Video] Phát hiện sớm bệnh nguy hiểm bằng chẩn đoán hình ảnh - Phần 2](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f52083899909c81ccf4c3aa38d2cb1b0b3410dc7892cff55400431bcae069a4acbd41a6c5eb84419e601652c0845f30bf7a25dd0d78c5f9ac818fb5639b9ba0160960f78/avatar-of-video-1169947-766.png.avif)
![[Video] Phát hiện sớm bệnh nguy hiểm bằng chẩn đoán hình ảnh - Phần 1](https://cdn.nhandan.vn/images/e53b3df5710fb57b6bbd10e5f52083899909c81ccf4c3aa38d2cb1b0b3410dc7892cff55400431bcae069a4acbd41a6ca372a3fad8c671cbbad9f775e32128e484e4521323f1eae7f68017a36356e093/avatar-of-video-1169944-1261.png.avif)